राउल्ट का नियम क्या है? इसका सूत्र, अनुप्रयोग, उदाहरण और सीमाएं

हेलो दोस्तों स्वागत है आपका हमारी हिंदी केमिस्ट्री की वेबसाइट परI आज हम आपको राउल्ट का नियम क्या है? राउल्ट के नियम का सूत्र क्या है, राउल्ट के नियम के अनुप्रयोग के बारे में बताइए और इसके साथ साथ हम राउल्ट के नियम की सीमाएं को भी बताएंगे। पिछले आर्टिकल में हमने आपको सांद्रता किसे कहते हैं इसके बारे में बताया और इसके साथ हमने विलयन, विलायक और सान्द्र विलयन के बारे में भी बताया। तथा इसके साथ साथ हमने सांद्रता व्यक्त करने वाली विधियों को भी बताया। जिसमें हमने आपको आयतन प्रतिशत, द्रव्यमान प्रतिशत, मोलरता, नार्मलता, मोल प्रभाज आदि के बारे में विस्तार के साथ बताया है।
आज के इस आर्टिकल में हम आपको राउल्ट के नियम के बारे बताएँगे। राउल्ट का नियम एक बहुत महत्वपूर्ण टॉपिक है जो परीक्षाओं में अक्सर पूछ लिया जाता है। जिसके बारे में हमें पता ही होना चाहिए कि राउल्ट का नियम होता क्या राउल्ट के नियम की सीमाएं क्या राउल्ट के नियम के उदाहरण क्या है? राउल्ट के नियम के अनुप्रयोग क्या है? इन सब सवालों के जवाब आपको पता होना चाहिए। इस टॉपिक से संबंधित प्रश्न कई बार बोर्ड परीक्षाओं में पूछे जा चुके हैं। इस आर्टिकल में हम आपको राउल्ट के नियम से संबंधित सभी जानकारी विस्तार के साथ देने वाले हैं तो चलिए शुरू करते हैं आज का टॉपिक राउल्ट का नियम।
राउल्ट का नियम क्या है?
राउल्ट का नियम फ्रांसीसी वैज्ञानिक राउल्ट ने 1887 में दिया था। इस नियम के अनुसार किसी विलयन के वाष्प दाब का आपेक्षित अवनमन विलयन में उपस्थित विलेय के मोल प्रभाज के बराबर होता है। या किसी विलायक में कोई अवाष्पशील विलय मिलाने पर विलायक के वाष्पदाब का आपेक्षित अवनमन विलयन में विलेय के मोल प्रभाज के बराबर होता है। इसे राउल्ट का नियम कहते हैं। अथवा किसी निश्चित ताप पर किसी अवाष्पशील विलेय युक्त विलयन का बाष्प दाब उसमें उपस्थित विलायक के मोल प्रभाज के समानुपाती होता है।
माना किसी अवाष्पशील विलयन का वाष्पदाब P तथा विलायक का वाष्पदाब PA है जो कि विलयन के वाष्पदाब के बराबर होता है। अतः राउल्ट के नियम के अनुसार –
Pi = XiPio
जहाँ Pio शुद्ध अवयव का वाष्प दाब है।
जब किसी विलयन के घटक साम्यावस्था में पहुँच जाते हैं उस स्थिति में राउल्ट का नियम एवं डाल्टन का आंशिक दाब का नियम को मिलाकर निम्न सूत्र को निकला जा सकता है।
P = P*XA + P*BXB + …
यदि हम दो द्रवों से बने विलयन से मिलकर बने विलयन के बाष्पदाब की (इसमें कोई और गैस उपस्थित न हो) तो के नियम के आधार पर इस विलयन के वाष्पदाब की गणना की जा सकती है। इस विलयन का कुल बाष्प दाब P दोनों विलयनो के शुद्ध वाष्पदाबो PA तथा PB के योग के बराबर होगा। अर्थात दोनों विलयनो के A व B का वाष्पदाब निम्नलिखित होगा।
P = P*AXA + P*BXB
क्योंकि सभी मोल अंशो का योग एक होता है अतः इसलिए
P = P*A(1 -XB) + P*BXB = P*A + (P*B -P*A)XB
इससे सिद्ध होता है कि दो द्रवों का सम्मिलित वाष्पदाब मोल प्रभाज XB का एक रेखिक फलन है।
यदि कोई अवाष्पशील विलय जिसका वाष्पदाब शून्य हो को किसी विलायक ,में मिलाया जाता है तो यह देखा गया है कि इस विलयन का वाष्पदाब शुद्ध विलायक के वाष्पदाब से कम होता है। जैसा की चित्र में दिखाया गया है।
इस नियम को निम्नलिखित समीकरण द्वारा लिखा जा सकता है।
Psolution = Χsolvent Pºsolvent
जहाँ Psolution विलयन का वाष्प दाब है।
Posolvent सुद्ध विलायक का वाष्प दाब है।
Xsolvent विलायक का मोल अंश है।
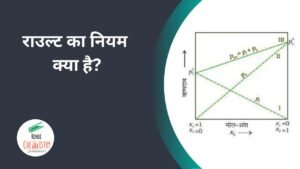
वाष्पशील विलायक मिश्रण
यदि आपके पास दो वाष्पशील विलायक A और B का मिश्रण हैं तो आप वाष्प के दाब की गणना कर सकते हैं। यह गैस A व B द्वारा लगाए गए आंशिक दाबों का योग होता है।
PA = XA * P Aº
PB = XB * P Bº
इस प्रकार हम A व B के दावों को जोड़ने पर हम कुल दाब P प्राप्त कर सकते हैं।
P = X A * PºA + XB * PºB
जहाँ जो P है बह विलयन के गैस दाबो का वाष्प दाब है। तथा XA व XB मिश्रण में अस्थिर विलायक A और B के मोल अंश हैं।
राउल्ट के नियम की सीमाएं
- राउल्ट का नियम विद्युत अपघट्य के विलयनो पर लागू नहीं होता है।
- राउल्ट का नियम केवल तनु विलयनो पर लागू होता है।
- सान्द्र विलयन में यह विचलन प्रदर्शित करता है।
- जो पदार्थ विलयन में संगुणित या वियोजित होते हैं वे इस नियम का पालन नहीं करते हैं।
राउल्ट के नियम के अनुप्रयोग
- राउल्ट के नियम का उपयोग किसी घोल के वाष्पशील घटक जैसे एथेनोल, एथेन, टालुईन, बेंजीन ,प्रोपेन आदि के वाष्पदाब की गणना के लिए किया जाता है।
- इसी तरह इस नियम से यह निर्धरित करना संभव है कि वाष्प के दवाव में क्या कमी हुई।
पूछे गए प्रश्न (FAQ) व उदहारण
प्रश्न- आदर्श विलयन किसे कहते हैं?
उत्तर- वह विलयन जो सभी संद्रताओं पर राउल्ट के नियम का पालन करते हैं। आदर्श विलयन (Ideal solution) कहलाते हैं।
- इस विलयन का Theoretical Pressure उसके Observed Pressure के बराबर होता है। Pth = Pobs
- वह विलयन जिसका आयतन परिवर्तन शून्य होता है उसे आदर्श विलयन कहते हैं।
- वह विलयन जिसमें उसका एनथेल्पी परिवर्तन शून्य होता है उसे आदर्श विलयन कहते हैं।
- एन-हेक्सेन और एन-हेप्टेन , वेंजीन और टालुइन का विलयन, ब्रोमो एथेन और क्लोरोएथेन का विलयन आदि आदर्श विलयन हैं।

प्रश्न- अनादर्श विलयन किसे कहते हैं?
उत्तर- वह विलयन जो सभी संद्रताओं पर राउल्ट के नियम का पालन नहीं करता है अनादर्श विलयन (Non Ideal Solution) कहलाता है। अर्थात इसमें Observe Pressure उसके Theoretical Pressure के बराबर नहीं होता है। यह दो प्रकार का होता है।
- धनात्मक विचलन दर्शाने वाला अनादर्श विलयन
- ऋणात्मक विचलन दर्शाने वाला अनादर्श विलयन
निष्कर्ष
दोस्तों आज के आर्टिकल में हमने आपको राउल्ट का नियम क्या है? राउल्ट के नियम की परिभाषा, राउल्ट के नियम की क्या क्या सीमाएं है? तथा राउल्ट के नियम के अनुप्रयोग कौन कौन से हैं? इसके बारे में बताया है। और इसके साथ साथ हमने आपको राउल्ट के नियम से सम्बंधित आदर्श विलयन किसे कहते हैं? और अनादर्श विलयन किसे कहते हैं इसके बारे में भी विस्तार के साथ बताया है। इसी तरह की केमिस्ट्री से सम्बंधित नई नई जानकारी प्राप्त करने के लिए जुड़े रहिए हमारी हिंदी केमिस्ट्री की इस वेवसाइट के साथ तब तक के लिए धन्यवाद।




